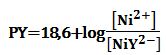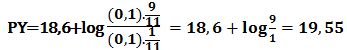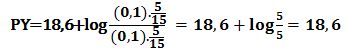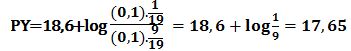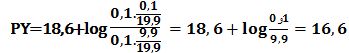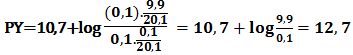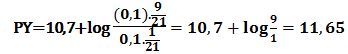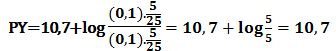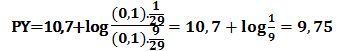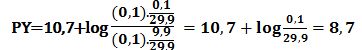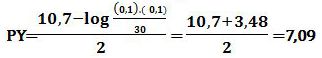E.D.T.A. منحنيات معايرة مزيج من شوارد معدنية بواسطة Calibration curves of a mixture of metallic ions by E.D.T.A.
E.D.T.A. منحنيات معايرة مزيج من شوارد معدنية بواسطة
يُمكن للشاردة السالبة -Y4 لمركب الإيتيلين ثنائي الأمين رباعي حمض الخل .E.D.T.A
الذي يُرمز له بـِ H4Y أن تتبادل بالكثير من الشوارد المعدنية +Mn
مشكلة شوارد معقدة من الشكل MY4-]n-4] .
إن الشاردة المعدنية +Mn التي تتفاعل أولاً مع الشاردة -Y4 هي تلك الشاردة التي تشكل المعقد الأكثر ثباتاً
ويُمكن معايرة كل شاردة معدنية كما لو كانت بمفردها في المزيج
حيث تكون نقاط التكافؤ منفصلة تماماً.
وتُعطى قيمة [-PY=-log[Y4 عند نقطة التكافؤ الأولى لمزيج من شاردتين متساويتين في التركيز بالعلاقة :
وهي علاقة مشابهة لعلاقة PH نقطة التكافؤ الأولى لحمض متعدد الوظائف أو لمزيج من حمضين متساويين في التركيز لدى تعديل الأول منهما.
تمرين ـ ارسم منحني معايرة 10cm3 من مزيج لشوارد الكالسيوم +Ca2 وشوارد النيكل +Ni2 تركيز كل منهما في المزيج 0,1N بواسطة محلول -Y4 تركيزه 0,1N أيضاً.
مع العلم أن ثوابت تفكك المعقدين هما PKd(Ni2+)=18,6 و PKd(Ca2+)=10,7 .
من قيم ثوابت التفكك تتفاعل شوارد النيكل +Ni2 أولاً مع -Y4 ويليها شوارد الكالسيوم +Ca2 .
إن 10cm3من محلول -Y4 يلزم لمعايرة كل من +Ni2 و +Ca2 ، لذلك يستهلك منه 20cm3 .
قبل بدء المعايرة: لا يمكن تحديد قيم PY لعدم تواجد -Y4 في وعاء التحليل.
خلال معايرة +Ni2 : تحسب قيم PY من العلاقة:
عند إضافة 1cm3 من -Y4 تتشكل كمية مكافئة من -NiY2 ويبقى في المزيج 9cm3 من شوارد النيكل دون تفاعل في حجم مقداره 11cm3 وبالتالي:
وعند إضافة 5cm3 من -Y4 تتشكل كمية مكافئة من -NiY2 ويبقى في المزيج 5cm3 من شوارد النيكل دون تفاعل في حجم مقداره 15cm3 وبالتالي:
وعند إضافة 9cm3 من -Y4 تتشكل كمية مكافئة من -NiY2 ويبقى في المزيج 1cm3 من شوارد النيكل دون تفاعل في حجم مقداره 19cm3 وبالتالي:
وعند إضافة 9,9cm3 من -Y4 تتشكل كمية مكافئة من -NiY2 ويبقى في المزيج 0,1cm3 من شوارد النيكل دون تفاعل في حجم مقداره 19,9cm3 ويكون خطأ المعايرة %0,1- :
:عند نقطة التكافؤ الأولى
:من العلاقة PY تُحسب قيم Ca2+ خلال معايرة شوارد الكالسيوم
عند إضافة 10,1cm3 من -Y4 ( أي 0,1cm3 بعد نقطة التكافؤ الأولى)تتشكل كمية مكافئة من -CaY2 ويبقى في المزيج 9,9cm3 من شوارد الكالسيوم دون تفاعل في حجم مقداره 20,1cm3 وبالتالي:
عند إضافة 11cm3 من -Y4 ( أي 1cm3 بعد نقطة التكافؤ الأولى)تتشكل كمية مكافئة من -CaY2 ويبقى في المزيج 9cm3 من شوارد الكالسيوم دون تفاعل في حجم مقداره 21cm3 وبالتالي:
عند إضافة 15cm3 من -Y4 ( أي 5cm3 بعد نقطة التكافؤ الأولى)تتشكل كمية مكافئة من -CaY2 ويبقى في المزيج 5cm3 من شوارد الكالسيوم دون تفاعل في حجم مقداره 25cm3 وبالتالي:
عند إضافة 19cm3 من -Y4 ( أي 9cm3 بعد نقطة التكافؤ الأولى)تتشكل كمية مكافئة من -CaY2 ويبقى في المزيج 1cm3 من شوارد الكالسيوم دون تفاعل في حجم مقداره 29cm3 وبالتالي:
عند إضافة 19,9cm3 من -Y4 ( أي 9,9cm3 بعد نقطة التكافؤ الأولى)تتشكل كمية مكافئة من -CaY2 ويبقى في المزيج 0,1cm3 من شوارد الكالسيوم دون تفاعل في حجم مقداره 29,9cm3 ويكون خطأ المعايرة %0,1-:
عند نقطة التكافؤ الثانية: تُعطى قيمة PY بالعلاقة:
وحيث أصبح حجم المزيج 30cm3 فإن:
بعد تجاوز نقطة التكافؤ الثانية: يُصبح في المزيج كمية فائضة من -Y4 فعند تجاوز نقطة التكافؤ بمقدار 0,1cm3 من -Y4،
أي لدى إضافة 20,1cm3 من -Y4 يبقى في المحلول 0,1cm3 من -Y4
ويُصبح حجم المحلول 30,1cm3 ويكون خطأ المعايرة عندئذ %1+:
ولدى إضافة 21cm3 من -Y4 يبقى في المحلول1cm3 من -Y4 ويُصبح حجم المحلول 31cm3 :
ولدى إضافة 25cm3 من -Y4 يبقى في المحلول5cm3 من -Y4 ويُصبح حجم المحلول 35cm3 :
ولدى إضافة 30cm3 من -Y4 يبقى في المحلول10cm3 من -Y4 ويُصبح حجم المحلول 40cm3 :
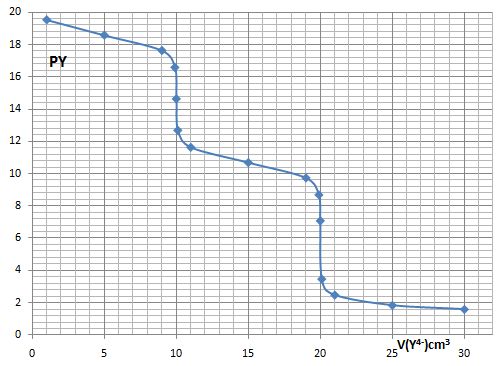
يُبين الشكل التالي منحني المعايرة:
إضافة تعليق
التعديل الأخير تم: 15/07/2021